브라이언 그린이 말하는 세상의 시작과 진화 그리고 끝

2. 시간의 언어 : 과거와 미래, 그리고 변화
시간을 정의하기 위해서 우리는 엔트로피를 알아야 한다. 엔트로피의 성질을 이해하기 위해선 열역학 제2법칙을 배워야 한다. 참 배울 것도 많다. 하지만 이것만 알면 세상이 돌아가는 이치를 많은 부분 이해할 수 있게 된다. 이왕 배우게 된 김에 열역학 제1법칙부터 알아보자. 열역학 제1법칙은 에너지 보존 법칙으로 에너지의 형태가 변화하더라도 에너지의 총량은 변함이 없음이란 뜻이다. 뜨거운 물에 얼음을 넣어서 미지근한 물이 된다고 해보자. 얼음은 미지근한 물로 형태가 변환했고, 뜨거운 물은 에너지가 줄어들었다. 그러나 에너지 소실이 없는 고립된 닫혀진 계에서의 에너지 총량은 같다. 얼음은 에너지를 얻고 물로 변환되었고 뜨거운 물분자는 열에너지(분자진동)를 잃어 미지근한 물이 되었다. 이것이 에너지 보존 법칙으로 열역학 제1법칙이다.
열역학 제2법칙은 어떤 형태의 에너지가 다른 에너지 형태로 변환될 때 완벽하게 변환되지 않고 일부 소실된다. 예를 들어 열에너지를 운동에너지로 전환한다고 할 때, 100% 에너지 전환(엔트로피 감소)하기 위해서는 외부 에너지가 필요하다. 아니면, 자체 에너지가 소실된다. 이것이 중요한 이유는 우리 우주에서는 모든 물질과 생명, 에너지는 열역학 제2법칙을 따르기 때문이다.
통계적 관점에서 살펴보자. 쉽게 말하면 엔트로피는 고립된 계에서 가장 높은 확율로 존재하고 있는 상태를 말한다. 무작위로 동전을 100개 던저셔 모두 앞면이 나오거나 모두 뒷면이 나올 확율보다 50개 앞면, 50개 뒷면으로 나올 확율이 더 높다. 그 상태가 엔트로피 평형 상태이다. 그런데, 어떤 외부 개입, 외력에 의해서 앞면 1개, 뒷면 99개가 나온다면 이는 나올 확율이 낮은 것이 나오게 되었으니 엔트로피는 감소하게 된 것이다. 여러 번 상자를 흔든다고 해보자, 흔들면 흔들수록 앞면 50개, 뒷면 50개로 높은 확율인 상태가 될 것이다. 이것이 저-엔트로피에서 고-엔트로피로 이동하는 것이다.

그러면 이 개념을 상자에 들어있는 입자들의 운동으로 치환해보자. 상자의 한 면을 부딪히는 입자들의 확율로 보고 정육면체 6면에 모두 동일한 확율로 입자들이 부딪힐 것이다. 이것은 모두 같은 면에서 압력이 동일하다는 것과 같은 내용이다. 만약 한쪽 면으로만 입자들이 몰려서 부딪힌다면 어떤 뜻일까? 이것은 존재하기 힘든 확율이므로 엔트로피는 감소하는 방향이다. 그리고 점유 공간의 부피도 줄어드니 엔트로피가 낮은 상태라고도 할 수 있다. 만약 상온에서 엔트로피 평형 상태일 때 상자를 압축한다면 어떻게 될까? 인위적으로 외부의 개입(외력)으로 입자들이 한 쪽면으로 압축되므로 엔트로피는 낮아지나, 입자들의 Mean Free Path가 짧아지게 되어 인자들의 진동은 커지게 되어 외부로 열에너지로 발산될 것이다. 외력이 주어진 것보단 작은 에너지로 열에너지가 전환된 것이다.
정리하면 입자 수가 작거나 온도가 낮거나 점유 공간의 부피가 작으면 엔트로피가 작은 상태이고, 입자 수가 많거나, 온도가 높거나, 점유공간의 부피가 크면 엔트로피는 크다. 그리고 일반적으로 엔트로피는 적은 상태에서 높은 상태로 흘러간다. 즉, 존재 확율이 낮은 상태에서 높은 상태로 흘러간다는 의미다. 동전 앞면 0개, 뒷면 100개에서 계속해서 던질 수록 50대 50이 나오는 상태가 그것이다.
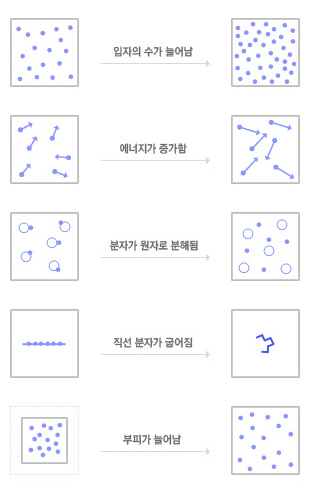
부연 설명으로 입자수가 적으면 면에 부딪힐 확율도 낮고, 온도가 낮으면 입자 운동 속도가 낮으므로 면에 부딪히는 속도도 낮고 확율도 낮다. 점유 공간의 부피가 크면 면에 부딪혀 재배열 될 확율이 낮으니 엔트로피가 낮다.
엔트로피 관련하여 항상 옳지는 않지만 경험에 비춰 볼 때 거의 사실에 가까운 명제를 하나 강조하고자 한다. 쉽게 말해서 우리가 경험하는 상태는 거의 대부분 엔트로피가 높은 상태라는 것이다. 고-엔트로피 상태는 구성 입자의 다양한 배열을 통해서 구현될 수 있으므로 전형적이고 평범하면서 흔한 상태이다. 존재할 수 있는 확율이 높은 상태를 말한다. 그리고 시간에 따라 엔트로피는 증가하는 경향이 있다. 자연현상에서 가끔 엔트로피가 감소하는 현상이 있긴한데 거의 대부분 증가하는 경향을 보인다.
엔트로피가 가장 높은 상태에 있지 않은 물리계는 장차 그 상태로 옮겨 갈 가능성이 매우 높다. 고-엔트로피에서의 가능한 입자의 배열 경우의 수는 저-엔트로피에서의 가능한 입자 배열 경우의 수보다는 압도적으로 많기 때문에 입자들이 무작위로 움직이다 보면 엔트로피가 높은 상태로 이동하게 된다. 이 변화는 엔트로피가 최대치에 도달할 때까지(가장 높은 확률인 상태) 계속되며, 최대 엔트로피에 도달한 후에는 무수히 많은 동일 배열(엔트로피가 같은 멤버들)사이를 왔다갔다하면서 최대 엔트로피를 유지한다.(확률적 안정화 상태) 이것이 열역학 제2법칙이며, 이 법칙이 성립하는 이유다.
모든 사건은 왜 한 쪽 방향으로만 진행되는 건인가? 물리 법칙은 과거과 미래를 차별하지 않는다는데, 왜 우리는 거꾸로 진행되는 사건을 볼 수 없는 것일까? 이 답은 열역학 제2법칙에서 찾을 수 있다. 엔트로피는 미래로 갈 때 증가할 확률이 압도적으로 높고, 그 역방향으로 진행될 확률(엔트로피 감소 확률)은 엄청나게 낮다. 그래서 시간은 거꾸로 흐르기 힘들다. 모든 사건이 거꾸로 가야 함은 그와 연결된 모든 입자와 그 운동이 확률이 낮은 방향으로 일제히 동시에 엔트로피가 낮은 방향으로 흘러야 한다. 한 사건에 대해서 외부 힘에 의해서 엔트로피를 낮추는 것은 가능하지만 모든 사건에 대해서 동시에 엔트로피를 낮추는 것은 불가능하므로 현실 세계에서는 시간이 거꾸로 흐르는 것을 볼 수 없다. 이는 우리의 노화의 시계도 거꾸로 되돌리고 다시 어려지는 현상이 벌어지며, 떨어져 깨어진 컵이 도로 붙는 것이 불가능한 것과 같다.
'Book Review' 카테고리의 다른 글
| 엔드 오브 타임 part4 [정보와 생명 : 구조체에서 생명으로] (0) | 2023.06.26 |
|---|---|
| 엔드 오브 타임 part3 [기원과 엔트로피 : 창조에서 구조체로] (0) | 2023.06.20 |
| 엔드 오브 타임 part1 [영원함의 매력 : 시작과 끝, 그리고 그 너머] (0) | 2023.06.10 |
| 지적 대화를 위한 넓고 얕은 지식 둘 (지대넓얕2) part5 [신비] (0) | 2023.06.06 |
| 지적 대화를 위한 넓고 얕은 지식 둘 (지대넓얕2) part4 [종교] (0) | 2023.06.02 |



